Anvendelsesområder
Behandling af migræneanfald med eller uden aura.
Dispenseringsform
Smeltetabletter. 1 smeltetablet indeholder 10 mg rizatriptan (som benzoatsalt).
Doseringsforslag
- Voksne. 10 mg.
- Vender symptomerne tilbage, til trods for god effekt af 1. dosis, kan en yderligere dosis gives inden for de næste 24 timer, forudsat at der går mindst 2 timer mellem de 2 doser.
- Maksimal døgndosis er 20 mg.
- Hos patienter i propranololbehandling er dosis 5 mg.
Bemærk:
- Smeltetabletterne lægges oven på tungen. Patienter med mundtørhed kan ikke anvende disse.
- Hvis 1. dosis ikke virker, vindes intet ved at gentage doseringen til samme anfald.
- Manglende erfaring vedr. børn og unge < 18 år og ældre > 65 år.
- Triptaner bør højst benyttes 9 dage pr. måned for at undgå medicinoverforbrugshovedpine.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-18 årErfaring savnes ved behandling af børn og unge under 18 år. Sikkerhed og virkning er ikke klarlagt. Der foreligger begrænsede data.
Håndtering
Lægges på tungen.
Efter opløsning i munden synkes med spyttet.
Kan opløses i en skefuld vand.
Kan tages med eller uden mad.
Virkningen forsinkes med ca. 1 time ved indtagelse sammen med mad.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler.
kontraindiceret |
|
|---|---|
| GFR | Advarsel |
| <10 ml/min. | |
Nedsat leverfunktion
- Forsigtighed ved let til moderat nedsat leverfunktion.
- Kontraindiceret ved stærkt nedsat leverfunktion.
Kontraindikationer
- Iskæmisk hjertesygdom
- Variant-angina/koronar vasospasme
- Tidligere myokardieinfarkt
- Tidligere cerebrovaskulært attak (CVA)
- Transitorisk cerebral iskæmi (TCI) i hjernen
- Moderat eller svær hypertension
- Mild ukontrolleret hypertension
- Symptomgivende perifere vaskulære lidelser
- Svær overfølsomhed for andre triptaner pga. risiko for krydsallergi
- Samtidig indgift af ergotamin, derivater af ergotamin, andre triptaner/5-HT1-receptoragonister eller MAO-hæmmere. Se interaktioner.
- Smeltetabletterne indeholder aspartam, der i organismen omdannes til fenylalanin. Denne dispenseringsform må derfor ikke anvendes til patienter med fenylketonuri (Føllings sygdom).
Forsigtighedsregler
- Patienter med epilepsi/nedsat krampetærskel
- Bør ikke gives til patienter i risikogruppen for iskæmisk hjertelidelse uden forudgående kardiovaskulær undersøgelse.
- Forsigtighed ved alvorlig overfølsomhedsreaktion for antibakterielle sulfonamider, fx dapson, sulfamethizol, sulfamethoxazol og sulfasalazin, selvom risikoen for krydsallergi er beskeden.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Hjerte | Palpitationer | |
| Mave-tarm-kanalen | Abdominalsmerter | Diarré, Dyspepsi, Kvalme, Mundtørhed, Opkastning |
| Almene symptomer og reaktioner på administrationsstedet | Kraftesløshed, Træthed, Tyngdefornemmelse, Varmefølelse | |
| Knogler, led, muskler og bindevæv | Rigiditet | Nakkesmerter |
| Nervesystemet | Hypæstesi, Paræstesier, Svimmelhed | Hovedpine |
| Psykiske forstyrrelser | Kognitiv dysfunktion, Somnolens | Søvnløshed |
| Det reproduktive system og mammae | Smerter i brysterne | |
| Luftveje, thorax og mediastinum | Dyspnø | Halsgener |
| Hud og subkutane væv | Rødme, Øget svedtendens | |
| Ikke almindelige (0,1-1 %) | ||
| Hjerte | Arytmier | Takykardi |
| Øjne | Synsforstyrrelser | |
| Mave-tarm-kanalen | Smagsforstyrrelser | |
| Immunsystemet | Angioødem | Urticaria |
| Undersøgelser | Ekg-forandringer | |
| Metabolisme og ernæring | Tørst | |
| Knogler, led, muskler og bindevæv | Muskelsvaghed | |
| Nervesystemet | Ataksi, Tremor | |
| Psykiske forstyrrelser | Konfusion, Nervøsitet | |
| Hud og subkutane væv | Hudkløe, Hududslæt | |
| Vaskulære sygdomme | Hypertension, Synkope | Hedeture |
| Sjældne (0,01-0,1 %) | ||
| Hjerte | Bradykardi | |
| Immunsystemet | Allergiske reaktioner (herunder anafylaktisk reaktion) | |
| Luftveje, thorax og mediastinum | Stridor | |
| Vaskulære sygdomme | Cerebrovaskulære tilfælde | |
| Ikke kendt hyppighed | ||
| Hjerte | Myokardieinfarkt, Myokardieiskæmi | |
| Mave-tarm-kanalen | Iskæmisk colitis | |
| Traumer, forgiftninger og behandlingskomplikationer | Serotoninsyndrom | |
| Knogler, led, muskler og bindevæv | Kramper | Myalgi |
| Hud og subkutane væv | Toksisk epidermal nekrolyse (TEN) | |
| Vaskulære sygdomme | Perifer iskæmi | |
Interaktioner
- På grund af risiko for vasokonstriktorisk effekt skal der gå 24 timer efter indgift af ergotamin før administration af triptaner. Omvendt skal der gå 6 timer efter indgift af triptan før administration af ergotamin.
- På grund af risiko for vasokonstriktorisk effekt og additiv effekt er kombination af rizatriptan og ergotamin, ergotderivater eller andre triptaner/5-HT1-receptoragonister kontraindiceret.
- Behandling med MAO-hæmmere inden for 2 uger inden behandling med rizatriptan forlænger og forstærker virkningen af rizatriptan.
- Propranolol øger plasmakoncentrationen af rizatriptan.
- Samtidig brug af SSRI, SNRI eller opioider giver risiko for udvikling af serotoninsyndrom.
- Bivirkningsfrekvensen kan øges ved samtidig brug af perikon.
Graviditet
Baggrund: Der er data for ca. 500 1. trimester-eksponerede uden tegn på overhyppighed af misdannelser. Den begrænsede datamængde tillader ikke at udelukke en øget risiko. Se endvidere Triptaner.
Se også: Klassifikation - graviditet
Amning
Baggrund: Den relative vægtjusterede dosis er under 1 %.
Bloddonor
Ingen karantæne ved tapning af plasma til fraktionering.
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Rizatriptan "Viatris" påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
- Virker vasokonstriktorisk på intrakranielle arterier og hæmmer frigørelse af peptider. Virkningen skyldes selektiv stimulation af 5-HT1B/1D-receptorerne.
- Virkningen indtræder efter ca. 0,5 timer (tabletter) og ca. 1 time (smeltetabletter).
Farmakokinetik
- Biotilgængelighed 40-45 %.
- Maksimal plasmakoncentration efter 1 time (tabletter) og 1,5 timer (smeltetabletter).
- Metaboliseres i leveren til ikke farmakologiske aktive metabolitter.
- Plasmahalveringstid 2-3 timer.
- Ca. 14 % udskilles uomdannet gennem nyrerne.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Smeltetabletter | 10 mg |
Smag
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | smeltetabletter
10 mg
Rizatriptan "Viatris" |
154905 |
6 stk. (blister)
|
282,10 | 47,02 | 47,02 | |
| (B) | smeltetabletter
10 mg
Rizatriptan "Viatris" |
480054 |
18 stk. (blister)
|
573,50 | 31,86 | 31,86 |
Substitution
| smeltetabletter 10 mg |
|---|
| Clurizcare (Parallelimport), Rizatriptan, smeltetabletter 10 mg |
| Maxalt Smelt Organon Denmark, Rizatriptan, frysetørrede tabletter 10 mg |
| Rizasmelt STADA Nordic, Rizatriptan, smeltetabletter 10 mg |
| Rizatriptan "Glenmark" Glenmark Nordic, Rizatriptan, smeltetabletter 10 mg |
| Rizatriptan "Sandoz" Sandoz, Rizatriptan, smeltetabletter 10 mg |
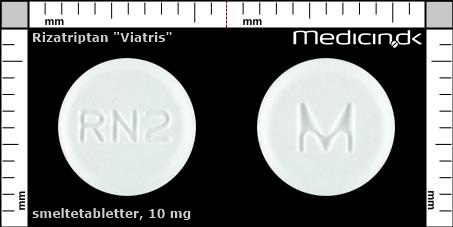
Foto og identifikation
Smeltetabletter 10 mg |
| Præg: |
RN2, M
|
| Kærv: | Ingen kærv |
| Farve: | Hvid |
| Mål i mm: | 8,3 x 8,3 |
Referencer
3711. Janusinfo. Janusmed (Fosterpåverkan). Region Stochholm. 2021, https://janusmed.se/fosterpaverkan (Lokaliseret 18. marts 2026)
6368. Amundsen S, Nordeng H, Fuskevåg OM et al. Transfer of triptans into human breast milk and estimation of infant drug exposure through breastfeeding. Basic Clin Pharmacol Toxicol. 2021; 128(6):795-804, https://pubmed.ncbi.nlm.nih.gov/33730376/ (Lokaliseret 25. marts 2026)
4255. Spielmann K, Kayser A, Beck E et al. Pregnancy outcome after anti-migraine triptan use: A prospective observational cohort study. Cephalalgia. 2018; 38:1081-92, https://pubmed.ncbi.nlm.nih.gov/28758416/ (Lokaliseret 25. marts 2026)
4252. Marchenko A, Etwel F, Olutunfese O. Pregnancy outcome following prenatal exposure to triptan medications: a meta-analysis. Headache. 2015; 55:490-501, https://pubmed.ncbi.nlm.nih.gov/25644494/ (Lokaliseret 25. marts 2026)
4251. Nezvalová-Henriksen K, Spigset O, Nordeng H. Triptan safety during pregnancy: a Norwegian population registry study. Eur J Epidemiol. 2013; 28:759-69, https://pubmed.ncbi.nlm.nih.gov/23884894/ (Lokaliseret 25. marts 2026)
3875. Nezvalová-Henriksen K, Spigset O, Nordeng H. Effects of codeine on pregnancy outcome: results from a large population-based cohort study. Eur J Clin Pharmacol. 2011; 67(12):1253-61, https://pubmed.ncbi.nlm.nih.gov/21656212/ (Lokaliseret 19. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



