Generel information
Glutamat N-methyl-D-aspartat (NMDA)-receptorantagonist. Middel til behandling af demens.
Anvendelsesområder
Anvendes ved Alzheimers sygdom, Lewy Body demens og demens ved Parkinsons sygdom i moderat til svær grad. Se endvidere Demens.
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder 10 mg (delekærv) memantinhydrochlorid.
Doseringsforslag
Voksne
5 mg 1 gang dgl. i den første uge. I den anden uge gives 10 mg 1 gang dgl. I den tredje uge gives 15 mg 1 gang dgl. Fra fjerde uge fortsættes med vedligeholdelsesdosis 20 mg 1 gang dgl.
Bemærk:
- Tabletterne tages med et glas vand.
- Tabletterne kan knuses. Knust tablet kan kommes på kold, blød mad.
- Tablet eller knust tablet kan opslæmmes i vand.
- Kan tages med eller uden mad.
- Dosis bør tages på samme tidspunkt hver dag.
- Patienten bør have en omsorgsperson (kan være fra hjemmeplejen), som hjælper med at håndtere medicineringen.
Håndtering af kapsler og tabletter
| filmovertrukne tabletter 10 mg, TEVA Delekærv |
Mad og drikke
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på kold, blød mad.
Knusning/åbning
Kan knuses.
Administration
Tablet eller knust tablet kan opslæmmes i vand.
Se endvidere Håndtering af tabletter og kapsler.
Nedsat nyrefunktion
Dosisjustering
- GFR: 0-30 ml/min.
- Alder: ≥17 år
- Dosis: >10 mg
Initialdosis 5 mg 1 gang dgl. Efter 1 uge evt. dosisøgning til højst 10 mg 1 gang dgl.
Beregn eGFR for patienter > 17 år: Beregning af eGFR ud fra CKD-EPI–formlen
Nedsat leverfunktion
Forsigtighedsregler
På grund af manglende erfaring anbefales forsigtighed ved:
- Epilepsi
- Nylig myokardieinfarkt
- Ubehandlet hjerteinsufficiens
- Ukontrolleret hypertension.
Hjælpestoffer
Tabletterne indeholder lecithin fra soja. Læs mere om soja og overfølsomhed.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Mave-tarm-kanalen | Obstipation | |
| Almene symptomer og reaktioner på administrationsstedet | Balanceforstyrrelser | |
| Lever og galdeveje | Leverpåvirkning | |
| Immunsystemet | Hypersensitivitet | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Psykiske forstyrrelser | Døsighed | |
| Luftveje, thorax og mediastinum | Dyspnø | |
| Vaskulære sygdomme | Hypertension | |
| Ikke almindelige (0,1-1 %) | ||
| Hjerte | Hjerteinsufficiens | |
| Mave-tarm-kanalen | Opkastning | |
| Almene symptomer og reaktioner på administrationsstedet | Kraftesløshed | |
| Infektioner og parasitære sygdomme | Svampeinfektioner | |
| Nervesystemet | Gangforstyrrelser | |
| Psykiske forstyrrelser | Hallucinationer*, Konfusion | |
| Vaskulære sygdomme | Trombose | |
| Meget sjældne (< 0,01 %) | ||
| Knogler, led, muskler og bindevæv | Kramper** | |
| Ikke kendt hyppighed | ||
| Mave-tarm-kanalen | Pancreatitis | |
| Lever og galdeveje | Hepatitis | |
| Psykiske forstyrrelser | Psykose | |
* Hallucinationer er set ved Alzheimers sygdom i svær grad.
** Generaliserede epileptiske anfald ("kramper") er hovedsageligt set hos patienter med epilepsi.
Kliniske aspekter
- Bivirkninger ved memantinbehandling er relativt sjældne, hyppigst er bivirkninger relateret til CNS som hovedpine, døsighed, konfusion og undertiden hallucinationer. Bivirkningerne vil ofte bedres ved fortsat behandling.
- Obstipation forekommer og håndteres på vanlig vis med bl.a. opmærksomhed på rigeligt væskeindtag.
- Balanceforstyrrelser ses og kan øge risikoen for fald.
Interaktioner
- Memantin kan forstærke virkningen af levodopa, dopaminerge agonister og antikolinergika, mens det muligvis kan nedsætte virkningen af barbiturater og antipsykotika.
- Samtidig behandling med amantadin, ketamin eller dextromethorphan skal undgås, idet disse stoffer påvirker samme receptorsystem som memantin med deraf følgende øget risiko for hyppigere og mere udtalte bivirkninger (bl.a. farmakotoksisk psykose).
- Ved samtidig brug af warfarin er der forekommet stigning i INR.
Graviditet
Der foreligger ikke kliniske data om eksponering for memantin under graviditet. Den potentielle risiko for mennesker er ukendt.
Amning
Ikke indiceret til ammende. Det vides ikke, om memantin udskilles i human mælk.
Bloddonor
Alkohol
Alkohol og Memantine "ratiopharm" påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
Farmakokinetik
- Biotilgængelighed ca. 100 %.
- Maksimal plasmakoncentration efter 3-8 timer.
- Steady state efter ca. 2 uger.
- Plasmahalveringstid 60-100 timer.
- Ca. 80 % udskilles uomdannet gennem nyrerne.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Udvalgte hjælpestoffer |
|---|---|---|---|
| filmovertrukne tabletter | 10 mg |
Farve
Andre
|
Firma
Tilskud
- Tabletter: Klausuleret tilskud til patienter med relevant demenssygdom i moderat til svær grad, hvor diagnosen er stillet af en speciallæge i psykiatri, neurologi og/eller geriatri. For de patienter, der opfylder klausulen, påtegnes recepten med ordet "tilskud".
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (A) | filmovertrukne tabletter
10 mg
(kan dosisdisp.)
Memantine "ratiopharm" |
107089 |
100 stk. (blister)
|
Udgået 23-06-2025 |
Substitution
| filmovertrukne tabletter 10 mg |
|---|
| Ebixa Lundbeck, Memantin, filmovertrukne tabletter 10 mg |
| Marbodin STADA Nordic, Memantin, filmovertrukne tabletter 10 mg |
| Memantin "Accord" Accord, Memantin, filmovertrukne tabletter 10 mg |
| Mentixa KRKA, Memantin, filmovertrukne tabletter 10 mg |
| Nemdatine Actavis, Memantin, filmovertrukne tabletter 10 mg |
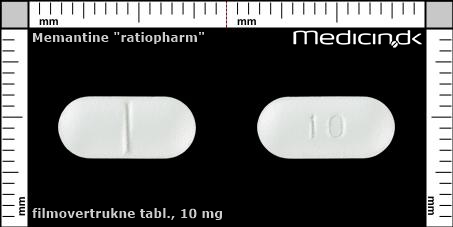
Foto og identifikation
Filmovertrukne tabletter 10 mg |
| Præg: |
10
|
| Kærv: | Delekærv |
| Farve: | Hvid |
| Mål i mm: | 5,6 x 12,5 |
Referencer
3800. pro.medicin.dk. 2025, https://pro.medicin.dk/ (Lokaliseret 5. maj 2025)
3801. Drugs.com. 2025, https://www.drugs.com/ (Lokaliseret 5. maj 2025)
3802. Micromedex. , https://www.micromedexsolutions.com (Lokaliseret 5. maj 2025)
3803. Produktresumeer. http://www.produktresume.dk, http://www.ema.europa.eu, https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm, https://www.medicines.org.uk. , (Lokaliseret 5. maj 2025)



